Sanofi, l’azienda farmaceutica con sede a Lione, in Francia, sta lanciando una grande campagna pubblicitaria per la vaccinazione contro il papillomavirus umano (HPV) . Questo potrebbe essere un contropiede innescato da una trentina di cause intentate contro il vaccino Gardasil progettato per prevenire il cancro cervicale e commercializzato da Sanofi-Pasteur MSD, dubbi sulla sua efficacia e il sospetto di conflitti di interesse?
La campagna pubblicitaria firmata da Sanofi è stata riportata nelle riviste femminili come Santé Magazine e Version Femina , leggendo a caratteri cubitali: “3028 casi di cancro cervicale e 40.000 lesioni cervicali. Ci sono modi per evitare questo. Chiedi al tuo medico “ .
Un vaccino controverso
Gardasil, un vaccino progettato per prevenire il cancro del collo dell’utero è stato venduto da Sanofi Pasteur MSD a partire dal 2006, ma le vendite sono crollate negli ultimi sei mesi. Il 31° di marzo, 420 medici hanno lanciato una petizione chiedendo a livello parlamentare che venga fatta luce sull’efficacia del vaccino in questione.
Cause intentate dalle vittime
All’inizio di aprile, l’europarlamentare Michèle Rivasi ha chiesto una moratoria sul Gardasil e l’avvio di una ricerca indipendente e trasparente sulla questione (leggi qui ). Al momento, ha invitato Marisol Touraine, ministro della Sanità francese, a “smettere di somministrare questo vaccino”.
Ad oggi, oltre trenta le cause depositate contro la Sanofi-Pasteur MSD, ai laboratori e ANSM ( Agence Nationale du Médicament ), all’agenzia del farmaco nazionale francese, attraverso l’unità di salute del TGI di Parigi ( Tribunal de Grande Instance ) , per “lesioni involontarie” (leggi qui ).
Le prime accuse penali contro questo vaccino sono state depositate il 22 ° di novembre 2013 da Marie-Océane Bourguignon che ha contratto encefalomielite acuta disseminata attribuita dai giudici ad una iniezione di Gardasil.
Conflitti di interesse
Alcuni esperti europei e francesi che hanno dato il loro consenso per l’autorizzazione della vaccinazione Gardasil, sono finanziariamente legati alla Sanofi e Merck.
Leggi l’articolo originale.
http://sanevax.org/sanofi-new-gardasil-advertising-campaign/
AMMISSIONE DI COLPEVOLEZZA SUL CONFLITTO DI INTERESSI RIGUARDO AL VACCINO HPV
La rapida approvazione della FDA riguardo il vaccino Gardasil.
Fino all’approvazione della FDA nel 2006, la Merck è stata pesantemente criticata per le sue strategie di marketing eccessivamente aggressive, attraverso campagne di lobbying finalizzate a promuovere il Gardasil come vaccino obbligatorio.
Successivamente, sono sorti i dubbi e domande sulla partecipazione dei produttori di vaccini alle politiche di salute pubblica, nonostante i loro conflitti di interesse così evidenti. Alcuni dei loro slogan della campagna pubblicitaria, come ad esempio “uccide il cancro cervicale” e “vostra figlia potrebbe diventare una vita in meno colpita da cancro cervicale,” sembravano progettati per promuovere la paura piuttosto che decisioni basate sulle evidenze sui benefici del vaccino.
Anche se, i conflitti di interesse non significano necessariamente che il prodotto stesso è difettoso, le rivendicazioni di marketing devono essere attentamente esaminate alla luce dei dati scientifici di fatto. Attualmente la vaccinazione Gardasil è fortemente raccomandata dagli Stati Uniti e da altre autorità sanitarie, mentre le preoccupazioni della popolazione, circa la sua sicurezza e l’efficacia,sembrano essere in aumento. Questa discrepanza porta ad alcune importanti questioni che devono essere risolte. L’attuale revisione esamina i temi chiave di questo dibattito alla luce delle attualmente disponibili evidenze della ricerca.
http://www.ncbi.nlm.nih.gov/pubmed/23061593
I conflitti di interesse nella ricerca sulla sicurezza del vaccino.
I Produttori di vaccini, i funzionari della sanità e le riviste mediche possono avere ragioni finanziarie e burocratiche per non voler riconoscere i rischi dei vaccini. Al contrario,altri,possono avere motivi legislativi e finanziari per sponsorizzare la ricerca che trova i rischi di questo vaccino. Utilizzando il dibattito vaccino-autismo come esempio, questo articolo descrive i conflitti di interesse di ciascuno,delineando lo stato attuale della ricerca sulla sicurezza del vaccino, e suggerisce i rimedi per affrontare il conflitto di interesse (COI).
http://www.ncbi.nlm.nih.gov/pubmed/22375842
CONFLITTI D’INTERESSE NELLA RICERCA BIOMEDICA E NELLA PRATICA CLINICA
14 aprile 2012
CONFLITTI D’INTERESSI NELLA RICERCA BIOMEDICA E NELLA PRATICA CLINICA Approvato nella Seduta Plenaria dell’8 Giugno 2006
Presidenza del Consiglio dei Ministri COMITATO NAZIONALE PER LA BIOETICA CONFLITTI D’INTERESSI NELLA RICERCA BIOMEDICA E NELLA PRATICA CLINICA Approvato nella Seduta Plenaria dell’8 Giugno 2006 (PDF)  Considerazioni finali
Considerazioni finali
Recentemente sono state descritte alcune delle situazioni che si vengono frequentemente a creare, nelle quali l’obiettività della ricerca e quella dell’informazione scientifica che viene data ai medici, può venir messa in pericolo:
1) l’industria spesso non fornisce ai medici un’informazione neutrale e completa, ma un’informazione già indirizzata, creata nei propri uffici;
2) i farmaci prodotti sono spesso duplicati di altri farmaci già esistenti (i cosiddetti farmaci me-too) che non presentano vantaggi rispetto a questi ultimi e che vengono venduti a un prezzo superiore.
L’industria promuove solitamente i medicamenti più recenti e costosi e a tal fine a volte elargisce ai medici vari tipi di “doni” che inducono nei sanitari un atteggiamento incline all’iperprescrizione o alla prescrizione dei farmaci più costosi;
3) l’industria controlla e indirizza la ricerca attraverso i finanziamenti che elargisce all’Università;
4) l’industria a volte interrompe ricerche non favorevoli o ne impedisce la pubblicazione. In altri casi distorce una ricerca in corso, sostituendo gli obiettivi (end points) primari con obiettivi surrogati;
5) i dati bruti delle sperimentazioni clinico-farmacologiche rimangono spesso nelle mani dell’industria e non vengono mai messi a disposizione dei ricercatori che li hanno prodotti. A questi ultimi i dati vengono forniti soltanto quando sono stati rielaborati dagli uffici statistici delle aziende;
6) l’industria, in quanto “proprietaria dei risultati”, non pubblica i risultati negativi;
7) le riviste scientifiche non pubblicano articoli con dati negativi perché di scarso interesse scientifico o commerciale;
8) l’industria condiziona, attraverso la pubblicità, le maggiori riviste mediche, i cui referees spesso hanno rapporti di dipendenza economica dalle aziende;
9) i medici che redigono le rassegne o le linee-guida sovente non sono davvero indipendenti dalle industrie;
10) anche le pubbliche amministrazioni spesso non sono indipendenti dalle industrie.
Questi comportamenti scorretti -peraltro non estensibili a tutte le industrie- non escludono che un regime di libero mercato correttamente inteso e regolato abbia avuto e possa avere un ruolo centrale nel progresso della ricerca biomedica e nello sviluppo delle tecnologie ad essa relative. Essi però possono creare condizioni di conflitto d’interesse nell’ambito dei ricercatori biomedici e dei clinici nei confronti delle aziende con le quali vengono in contatto.
Dichiarazione del Dr. Thomas Jefferson, Responsabile degli studi sui vaccini della COCHRANE ( la maggiore Agenzia di Revisione degli Studi Scientifici al mondo ):
“Prima di iniziare qualsiasi intervento ( TV o giornalistico o in qualsiasi riunione divulgativa ) ciascuno dovrebbe dichiarare la propria posizione riguardo a possibili CONFLITTI di INTERESSI, ed eventualmente dire se lavora o meno per AZIENDE FARMACEUTICHE: altro è il parere LIBERO, OGGETTIVO e SPASSIONATO di chi NON riceve fondi, finanziamenti, rimborsi o donazioni da esse.”
http://www.governo.it/bioetica/testi/Conflitti_interessi.pdf
VACCINO HPV PAPILLOMA VIRUS
Le origini dello scandalo: una galassia di conflitti di interesse.
Vaccino contro il cancro della cervice dell’utero: una bomba di salute
Il 04/01/14
Il Vaccino contro l’HPV è ora oggetto di diverse denunce penali, una recente petizione per una missione parlamentare e un appello per una moratoria.
Probabilmente l’inizio di una lunga storia medico-legale.Un nuovo scandalo in prospettiva.Otto anni più tardi, prove in attesa, forti sospetti sulla sua nocività, “grazie” alla sperimentazione pubblica.
Eppure,per il Piano di cancro 2014-2019, l’obiettivo della Francia è quello di raggiungere una copertura del 60%! Nonostante tutti i governi riconoscano la sua “inefficienza” della mortalità da cancro cervicale,non riuscendo a riconoscerne gli effetti nocivi e dannosi.

Come siamo arrivati fin qui? La risposta è la stessa di altri scandali sanitari; ricerche e studi scientifici correlati al conflitto di interesse,oltre alla codardia politica.Risultato: migliaia di giovani ragazze che hanno riscontrato gravi effetti collaterali, e nell’indifferenza generale. Storia di una catastrofe sanitaria annunciata.

Ovviamente tutto questo non è vero secondo la Sanofi Pasteur MSD. Continua affermando che il vaccino è raccomandato anche dall’OMS, dalle autorità sanitarie americane (FDA), l’Agenzia europea del farmaco,perciò sicuro.
Il Vaccino HPV e le sue origini.
Il Gardasil è indicato da 9 anni, per la prevenzione delle lesioni genitali precancerose del collo dell’utero, della vulva e della vagina ; per ridurre e combattere il cancro della cervice provocato dal Papillomavirus Umano, e per la prevenzione dei condilomi genitali (condilomi acuminati) causati da tipi di HPV specifici (6, 11).
In Francia, il Consiglio superiore della sanità pubblica (HCSP) raccomanda la vaccinazione delle ragazze tra gli 11 e i 14 anni. Si raccomanda inoltre di effettuare la vaccinazione entro i 20 anni, poichè è più efficace. I Centri statunitensi per il Controllo delle Malattie e la Prevenzione (CDC) raccomandano la vaccinazione anche per i ragazzi della stessa età,per frenare la trasmissione sessuale del virus, “responsabile di altri tipi di cancro” (tra cui il cancro del anale e alcuni tipi di cancro della testa e del collo).
Farmacovigilanza: “Niente da segnalare”
Ci sono sempre stati gli effetti collaterali con i vaccini, come qualsiasi altro farmaco. Nel caso del vaccino contro il cancro della cervice dell’utero, “sono lievi e transitori con una predominanza di dolore al sito di iniezione,” perciò,nessun motivo per allarmarsi così.
Questo è certamente ciò che emerge dal monitoraggio internazionale della farmacovigilanza, elenco degli effetti collaterali derivanti dalla commercializzazione di un farmaco.
Si,naturalmente, ” è stato segnalato qualche isteria epidemica come vertigini e sincope.” Ma «potremmo evitare questi eventi negli adolescenti per i primi 15 minuti di osservazione dopo la vaccinazione e incoraggiarli a rimanere idratati . ”
Le ragazze che arrivano in ospedale riportando malattie autoimmuni o finendo su una sedia a rotelle? morti? Pura coincidenza …
Questo vaccino è strettamente monitorato,come mai? Per tre ragioni: a causa del potenziale rischio di malattie autoimmuni, a causa di dati insufficienti,e a causa della mancanza di dati sulla sicurezza della vaccinazione a lungo termine.
Ma i rapporti periodici della salute sono rassicuranti: “I risultati delle analisi intermedie (novembre 2011) mostrano che l’impatto del tasso di malattie autoimmuni osservate in soggetti vaccinati con un vaccino HPV, non sono significativamente diversi da quelli osservati nei non vaccinati “. Conclusione: nulla, nulla da segnalare. Affermazioni sul Gardasil dalle case produttrici.
In un articolo francese, il Dr Bernard Guerin Masgenêt, ginecologo presso l’ospedale di maternità Gustave Dron a Tourcoing (Francia) ha dichiarato nel 2008, : «Non sarebbe la prima volta che le società scientifiche di Ginecologia, o di altre specialità, diano supporto scientifico ai laboratori farmaceutici. Indipendenza, interessi finanziari o di altro tipo non fanno ancora parte della nostra cultura medica! Nel mio caso,il Gardasil mi è stato “presentato” e spiegato, da un professore di ginecologia, accompagnato da un rappresentante del laboratorio … Tutti i prescrittori sono sotto una pressione significativa da parte dell’industria farmaceutica, la quale dirige gran parte della formazione post-laurea dei medici attraverso fondi. “
Le Varie Segnalazione di eventi avversi
“Nel caso del vaccino contro il cancro della cervice dell’utero, sono convinto che ci sia una forte sottostima che riporta il numero di casi di effetti collaterali” , assicura il Dr. Philippe De Chazournes. Il medico è presidente e fondatore dell’Associazione Med’Océan , che lavora da quasi 15 anni per l’indipendenza e la qualità delle informazioni mediche . ” Spesso è quasi impossibile fare il collegamento tra il tempo di iniezione e le reazioni avverse, che di tanto in tanto si verificano dopo diversi mesi. “
Tra l’1% e il 10% delle reazioni avverse sono riportate dal sistema di farmacovigilanza negli Stati Uniti. Uno studio francese, condotto tra il 1994 e il 1996 su anafilassi perioperatoria, ha stimato che solo il 13% dei casi sono stati segnalati al sistema di farmacovigilanza . Per avere una visione realistica degli effetti collaterali ,si dovrebbero quindi, riportare tutti i dati di segnalazione.
Ufficialmente, la Francia, secondo l’Agenzia nazionale per i medicinali, ha avuto 435 casi di eventi avversi gravi tra cui 135 malattie autoimmuni;15 casi di SM sono stati riportati dalla rete di farmacovigilanza nazionale, con più di 5 milioni di dosi di vaccino Gardasil (tra il 2006 e il maggio 2013).
Il tasso di denuncia (tutti gli effetti compresi) è quindi solo 38 per 100 000 dosi di vaccino, e il tasso dei gravi effetti avversi è di 8 per 100 000 dosi di vaccino. Ma questa cifra è veramente affidabile?
Niente è sicuro se ascoltate le testimonianze dei pazienti. Nella maggior parte dei casi, i loro medici non li ascoltano, non prendono sul serio i loro sentimenti e quindi non si preoccupano di effettuare una denuncia alle autorità sanitarie. ( fine articolo sono riportate le fonti delle testimonianze).
Un potenziale e lampante tossicità
Tra i gravi effetti indesiderati dopo la vaccinazione con Gardasil e Cervarix, molte sono le malattie autoimmuni classificate: artralgia / artrite / artropatia, tiroidite autoimmune, malattia celiaca e la malattia infiammatoria intestinale, diabete mellito, eritema nodoso, sclerosi multipla, infiammazioni renali, porpora trombocitopenica immune, psoriasi, fenomeno di Raynaud, artrite reumatoide, lupus eritematoso sistemico, e tante altre.
Inoltre sono stati segnalati casi di disturbi dell’equilibrio, udito, vista, pancreatite, encefalite, o trombosi venosa, talvolta fatali.
Tra i gravi casi segnalati, sono riportati anche danni alla funzione riproduttiva.
“Il British Medical Journal (BMJ) ha pubblicato il caso di una giovane australiana di 16 anni in perfetta salute,danneggiata a seguito del vaccino Gardasil,riporta il sito Citizen Initiative . Prima del menarca, questa ragazza è andata in uno stato di piena menopausa, le ovaie in fase di ultimazione per funzionare. “I genitori di Deidre, Teresa Harvey e Rodrick Greenville Ward, hanno direttamente richiamato l’attenzione sul fatto che,la ragazza era stata completamente esaminata.
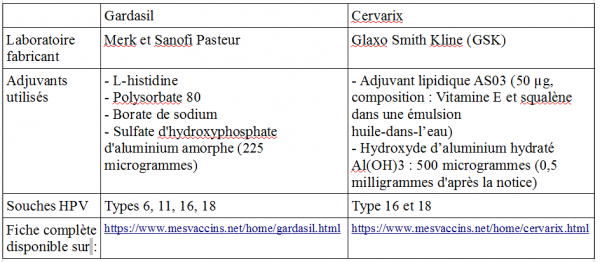
La tossicità del vaccino; i coadiuvanti HPV
| Alluminio idrossido (o fosfato amorfo o idrossifosfato solfato) Funzione:. coadiuvante immunità Promemoria: il massimo standard per l’acqua potabile è di 100 microgrammi per litro.Una iniezione di Gardasil contiene 225 Cervarix 500 microgrammi, che si trovano nel corpo senza aver attraversato le barriere naturali (ad esempio la digestione). |
Coinvolto nella malattia di Alzheimer, Parkinson nella sclerosi laterale amiotrofica (SLA) e altre degenerazione neurologica. Secondo Hugh Fudenberg immunogénéticien Herman, specialista autismo, un individuo che ha ricevuto 5 consecutivi vaccini contro l’influenza 10 volte più probabilità di avere il morbo di Alzheimer che non vaccinati. Il professor Gherardi (Bordeaux) attribuito anche al di alluminio vaccino “myofasciitis macrofagi.” I suoi studi forniscono una base scientifica per la denuncia dei pazienti nel gennaio 2013 contro Sanofi Pasteur. La denuncia comporta la presenza di alluminio nel vaccino REVAXIS ®, che ha sostituito l’obbligo DTP in precedenza senza alluminio!). Per saperne di più circa i pericoli di alluminio, è tutto nello studio del Dr. Jean Pilette (1.700 riferimenti scientifici) www.alis-france.com/download/alu_vaccins.pdf |
| Squalene (ASO3) Funzione: Questo non è un adiuvante in sé, ma migliora la risposta immunitaria. |
Sebbene squalene è una sostanza naturale del corpo, l’iniezione provoca la creazione di anticorpi contro lo squalene. Gli stessi anticorpi sono stati trovati nei portatori della sindrome della guerra del Golfo, con alcuni lotti vaccinati contro l’antrace vaccino contenente squalene (“Gli anticorpi anti-squalene nei destinatari del vaccino contro l’antrace” in E Xperimental e patologia molecolare 2002 Agosto; .. 73 (1) :19-27 Questa sindrome è caratterizzata da problemi renali e respiratori, cancro, disturbi del sistema nervoso, la leucemia, eruzioni cutanee Lo squalene è stato utilizzato nel contestatissimo vaccino contro l’influenza A. |
| L-istidina Funzione: come squalene, migliora la risposta immunitaria. |
L-istidina è un precursore di istamina che scatena una risposta infiammatoria nelle reazioni allergiche. Questo è un amminoacido chiamato “essenziale”. Fa parte degli oli usati (come squalene) come adiuvanti di indurre la malattia autoimmune in animali da esperimento in modo che possano essere studiati per eventuale trattamento di questi iniezione troubles.L L- istidina potrebbe causare una malattia autoimmune in cui la L-istidina viene attaccato dal sistema immunitario, con conseguente scarsità, causando molti disturbi 21 . |
| Polisorbato 80 Funzione: emulsionanti (presenti anche in gelati o cosmetici). |
Polisorbato 80 è noto per provocare shock allergico, ma anche distorsioni e follicoli ovarici degenerative, cambiamenti ormonali, cambiamenti nella dell’utero e della vagina nei ratti. Si tratta di un topo di sterilizzazione … Un elenco di studi sulla tossicità di questo emulsionante è disponibile in questo articolo: “polisorbato 80 e infertilità: un emulsionante che possono danneggiare la funzione riproduttiva” (polisorbato 80 cause di infertilità, un emulsionante che può danneggiare la salute riproduttiva) in inglese sul www.whale.to / vaccino / polysorbate.html |
| Borato di sodio Funzione: antisettico. |
Dal 6 novembre 2008, sali di boro sono classificati dalla normativa europea come tossici.Imballaggio prodotti, tra cui devono recare un logo per questo scopo teschio e ossa incrociate con le seguenti due indicazioni: R60 (può ridurre la fertilità) e R61 (rischio per la gravidanza di danni ai bambini). Questo è uno dei principali componenti del veleno per topi … Un tale conservante nei vaccini contro le infezioni della cervice è particolarmente preoccupante alla luce degli studi pre-clinici per l’immissione sul mercato :. Cinque donne sono rimaste incinte 30 giorni dopo la vaccinazione erano bambini anormali, come riportato nel parere del comitato tecnico per la vaccinazione vaccinazione contro il papillomavirus umano 22 |
Morti negli Stati Uniti
Negli Stati Uniti, la polemica sul Gardasil è molto forte. Alimentata da blog, testimonianze sui forum, associazioni in difesa delle vittime. Informatori seguono da vicino gli ultimi dati VAERS (Vaccine Adverse Event Reporting System), il registro di farmacovigilanza.
Sono davvero inquietanti, soprattutto quando si sa che sono probabilmente meno del 10% della realtà riporta le cifre “ufficiali” .
Vittime del vaccino contro l’HPV negli Stati Uniti – dicembre 2013 (Fonte VAERS)
| Descrizione |
Numero di VAERS |
Stima Probabile 24 tenendo conto sotto-segnalazione |
| Infermi |
1025 |
10250 |
| Morte |
155 |
1500 |
| I pazienti non guariti |
6549 |
65500 |
| Striscio anormale |
554 |
5540 |
| Displasia cervicale |
233 |
2330 |
| Il cancro cervicale |
71 |
700 |
| Vita minacciata |
600 |
6000 |
| Emergenza |
11148 |
111480 |
| Ricovero |
3367 |
33367 |
| Lunga degenza in ospedale |
244 |
2440 |
| Gravi condizioni |
4477 |
44770 |
| Effetti indesiderati rilevati |
32995 |
329.950 |
Ufficialmente, in Francia, non c’è una sola morte a causa di vaccino. Stranamente, gli Stati Uniti, che già se ne contavano 155. Sono stati distribuiti ,oltrepassando l’atlantico,ben 57 milioni di dosi tra il 2006 e il 2013 , contro 5.000.000 in Francia. La scienza statistica, dovrebbe tenere in considerazione il fenomeno della sotto-segnalazione.
Le prime denunce penali. Il primo caso,quello di Landes, Marie-Oceans
La circolazione del Gardasil è già uno scandalo per molti medici e scienziati che erano indignati nel 2006. Ma non lo è stato fino alla fine del 2013, fino a che il Gardasil è diventato un “caso” per i media. Dopo anni di controversia scientifica sul vaccino, il tempo è ora componente legale.
La prima denuncia è stata depositata 22 novembre 2013 da una giovane, Landes, Marie-Oceans . Si basa su una perizia, segnalando che il vaccino, stimolando l’immunità della giovane donna, abbia in realtà avviato una serie di eventi,causando l’infiammazione del sistema nervoso centrale .
Marie-Ocean e il suo avvocato hanno informato il laboratorio Sanofi Pasteur MSD sui rischi del Gardasil,sui rischi di infiammazioni centrali (mentre questi rischi sono stati individuati a partire dal 2009) del sistema nervoso, a seguito di una segnalazione delle reazioni avverse. Essi hanno inoltre accusano il MSNA aver preso alcuna azione contro il laboratorio.La storia di Marie-Ocean inizia nel settembre 2010, durante una visita al suo medico di famiglia per un certificato di pratica di danza. Secondo la “raccomandazioni ufficiali” il dottore “ha approfittato” per prescrivere la vaccinazione Gardasil. Quindici giorni dopo la prima dose,la ragazza sentiva “formicolio alle braccia e alle gambe.” Dopo la seconda,ottenuta verso la metà del dicembre 2010,era in preda a forti vertigini. Marie-Ocean finirà su una sedia a rotelle, cieca e quasi sorda. Oggi, la sua condizione sembra essersi stabilizzata. La Diagnosi medica si ripartisce in encefalomielite disseminata acuta (ADEM) o un primo attacco di sclerosi multipla (SM). “In seguito a questa denuncia, abbiamo ricevuto una cinquantina di testimonianze.E ogni ora, ci sono una dozzina di famiglie che comunicano, spiegando il loro disagio “ dice l’avvocato .
Nuove denunce sono state presentate da nove giovani,di età compresa tra 18-24 anni che vivono ovunque in Francia, ” hanno comunemente contratto malattie gravemente invalidanti nelle settimane e nei mesi successivi alla vaccinazione. ” Cinque di loro hanno contratto la malattia di Guillain-Barré; una, vittima della miastenia grave, e ipersonnia idiopatica ultimi soffre, secondo il testo della denuncia.
Verità scientifica: l’autorizzazione dubbia
Informatori ,molti medici, e siti come Citizen Initiative Pharmacritique , hanno ricercato molto sull’argomento. Tutti ricordano,le affermazioni del dottor Philippe De Chazournes,sulla inefficacia della prevenzione del cancro della cervice dell’utero dalla vaccinazione HPV.
A proposito di Gardasil,ecco l’ analisi critica e indipendente, di molti medici,basandosi su dati scientifici:
- L’efficacia del vaccino contro il cancro della cervice dell’utero non è provata oltre i 5 anni. Anche le autorità sanitarie riconoscono.
- Il vaccino non protegge contro tutti i tumori della cervice, ma solo contro due ceppi di HPV.L’affermazione che il vaccino potrebbe prevenire il 70% dei tumori è del tutto sbagliato. Questa è una percentuale ridicola rispetto alle prestazioni di rischio (quasi il 100%), soprattutto se si considera il costo della vaccinazione (prestazioni medico-economica): ci vogliono circa 400 € per i tre iniezioni, a scapito di sicurezza sociale e reciproca. “Questo è il più costoso nella storia della vaccinazione vaccino”, dice il Dott. Jean-Pierre Spinosa, ginecologo a Losanna. La valutazione medico-economica è stata effettuata sulla base del rendimento del 70%.
- Gli Studi di laboratorio indugiano troppo sulle prime lesioni cervicali, spesso benigne, che possono regredire naturalmente, molto prima della fase di un eventuale cancro. Quando si guarda da vicino i tassi delle lesioni cervicali precancerose,evince che sono più numerose nel gruppo vaccinato.
- Le Lesioni cervicali nelle giovani donne che hanno già ricevuto le dosi del vaccino sono superiori del 63% tra i vaccinati; alla fine, il vaccino provoca più danni con i virus 6, 11, 16 e 18 nel gruppo vaccino.
- Altri ceppi di HPV possono prendere il posto del cancro dopo la vaccinazione contro i ceppi vaccinali. Così, nel gruppo di soggetti vaccinati, ci sono 43% di CIN 3 di lesioni causate da altri ceppi di HPV rispetto al gruppo non vaccinato. Si parla di trasferimento della malattia.
- La sicurezza del vaccino nel lungo termine è completamente sconosciuta.
- Il Placebo utilizzato per valutare la tossicità dei vaccini non è placebo, perché contiene gli adiuvanti dei vaccini (alluminio). Quando si sa che l’alluminio è appunto coinvolto nei gravi effetti avversi, questi placebo non forniscono alcuna base per il confronto.
- I Laboratori alla fine effettuano studi “sabotati” ; la vaccinazione segue riferimenti di protocollo.
Infine, il vaccino HPV non avrebbe mai dovuto arrivare sul mercato. “Non perché sono potenzialmente dannosi (anche se è il caso), ma soprattutto a causa del maggior rischio di lesioni pre- cancro (CIN 2/3). Se questi vaccini non meritavano di autorizzazione sul mercato (AMM), è perché hanno fallito nella Fase III per dimostrare la loro efficacia nella prevenzione di tutte le CIN 2/3. E’ qui che c’è il profitto.
Le origini dello scandalo: una galassia di conflitti di interesse
Lo Scandalo Gardasil promette di essere una bomba a orologeria: una bomba a causa degli effetti collaterali sulla popolazione, ma anche una bomba legale a causa del numero di denunce. Si stima che i costi di vaccinazione in Francia siano di circa 100 milioni di € all’anno, pagati attraverso i contributi previdenziali, e dai cittadini. Dal 2006, l’inizio di questa vaccinazione, si è avvicinata così a 1000000000 € spesi, che sono balzati direttamente nelle tasche dei laboratori e dei proprietari dei brevetti. Il Prezzo della sanità sembra altrettanto grande quando si conosce il costo delle malattie a lungo termine, ricoveri in ospedale, consultazioni e prescrizioni, a seguito di effetti collaterali di questo vaccino.
In diversi articoli, descrive i rami tentacolari della lobby farmaceutica il Premio Nobel per la Medicina nel 2008. (“Gardasil e Cervarix: Astra Zeneca e la Fondazione Nobel sospettato di corruzione e conflitti di interesse in assegnazione del premio Nobel a Harald zur Hausen “ ) : “Il premio Nobel assegnato a Harald zur Hausen dovrebbe premiare la ricerca su HPV, ma soprattutto dedicato al trionfo dei conflitti di interesse che affliggono il Gardasil e Cervarix dal concepimento,contrariamente al loro dovere di salute pubblica.
“Questo premio è tempestiva per salvare il Gardasil in Germania … L’ubiquità di conflitto di interesse in materia di Gardasil e Cervarix è conosciuto in Germania per l’immissione sul mercato di Gardasil.
“Il coinvolgimento del laboratorio Astra Zeneca va alla ricerca di finanziamenti da parte della tedesca Harald zur Hausen ,ed è inseparabile dal conflitto di interessi DKFZ. Ecco ciò che il centro di ricerca tedesco ha finalmente riconosciuto in una newsletter del 2006, quando il DKFZ ha accolto con favore l’approvazione del Gardasil negli Stati Uniti:
“La strada verso il vaccino è infida. Durante i primi anni ’90, ci sono stati diversi gruppi di ricercatori che lavorano sulla vaccinazione HPV, insieme con il team di DKFZ. L’industria farmaceutica tedesca non ha mostrato interesse per queste ricerche critiche. Ed è per questo che il DKFZ ha diritti di licenza alla società di biotecnologia statunitense MedImmune (di proprietà di Astra Zeneca, ndr.) Riconoscendo il potenziale di un vaccino contro l’HPV, MedImmune,ha acquistato la licenza con altri istituti di ricerca, tra cui il National Institutes of Health (NIH) a Bethesda e Loyola University Chicago. D’altra parte, la società farmaceutica Merck ha acquistato i diritti per la licenza,i quali restano a loro (come quelle ancora detenute dal NIH e l’Università di Queensland in Australia)”.
“Merck e MedImmune hanno continuato il finanziamento della ricerca clinica, e i GSK entrarono in scena con l’acquisto della licenza da MedImmune. Gli studi di Fase III potrebbero iniziare nel 2005. All’inizio del 2005, Merck e GSK hanno assegnato ,licenze incrociate per l’uso reciproco dei brevetti. Allo stesso tempo, gli istituti di ricerca hanno raggiunto un accordo sui brevetti. “Dopo difficili negoziati, il DKFZ è stato confermato come co-titolare del brevetto con il NIH e sarà in grado di godere dei benefici finanziari Marketing [Gardasil e Cervarix] di Merck e GSK. In questo modo, i ricercatori, i centri di ricerca, imprese, e in particolare i pazienti potranno beneficiare del successo dei vaccini. “
Per informazioni, nel 2012, Gardasil ha registrato 1,2 miliardi di dollari per Merck e Cervarix 800 milioni di GSK … La figura è in crescita come gli Stati Uniti, secondo JAMA , il tasso di copertura vaccinale per le ragazze è importante (il 54% ha ricevuto almeno una dose nel 2012, il 33% tre iniezioni). Le Vendite di Gardasil dovrebbero superare i 1,8 miliardi dollari nel 2013 , con un incremento del 50% rispetto al 2009. Se i tassi di vaccinazione HPV aumento dei livelli di altri vaccini, ricavi Gardasil potrebbe raggiungere quasi 3 miliardi di dollari nei prossimi anni.
Per i laboratori, è chiaro, la vaccinazione deve andare avanti
Articoli correlati
- HPV: Gardasil ritiro …
- H1N1: nessuna indagine europea
- Silenzio su Cervarix
http://pryskaducoeurjoly.com/actu/1417/vaccin-contre-le-cancer-du-col-de-luterus-une-bombe-sanitaire-dossier
 (78 kb)
(78 kb) (620 KB)
(620 KB)